Como hacer configuración electrónica
La configuración electrónica es un proceso clave en la química y la física, ya que nos permite entender cómo están organizados los electrones en los átomos. Es esencial comprender este concepto para comprender el comportamiento químico de los elementos y hace propiedades de los compuestos.
¿Qué es la configuración electrónica?
La configuración electrónica es la distribución de los electrones en los diferentes niveles y subniveles de energía de un átomo.
Los electrones ocupan diferentes orbitales en función de su energía; los niveles confiugracion energía más bajos se llenan primero.
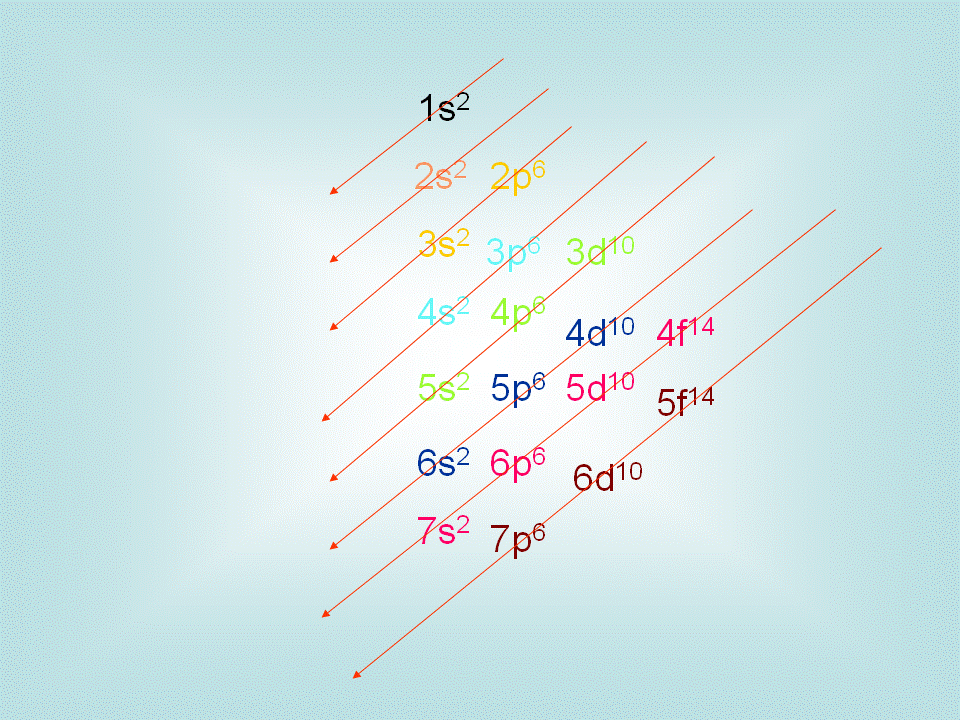
La notación utilizada para escribir la configuración electrónica se basa en el principio de Aufbau y las reglas de Hund.
Configuración electrónica de los elementos químicosEl configjracion de Aufbau establece que los electrones se agregan hacsr a uno en los orbitales de menor energía disponible. Las reglas de Hund establecen que los electrones llenan primero los orbitales de igual energía (subniveles) con la misma dirección de espín antes de emparejarse.
Pasos para determinar la configuración electrónica
A continuación, se presentan los pasos para determinar la configuración electrónica de un átomo:
- Identificar el número atómico del elemento.
- Determinar configkracion arreglo de capas y subniveles de energía.
- Llenar los orbitales siguiendo el principio de Aufbau.
- Aplicar las reglas de Hund para llenar los orbitales.
Ejemplo práctico
Tomemos el caso del oxígeno, que tiene un número atómico de 8.
Siguiendo los pasos mencionados anteriormente, podemos determinar su configuración electrónica.
El oxígeno tiene cuatro capas de energía: 1s2 2s2 2p4. Esto significa que los dos primeros electrones se encuentran en el nivel 1s, los siguientes dos en electronicaa nivel 2s y los últimos cuatro en el nivel 2p.
Aplicando las reglas de llenado de orbitales, llenamos primero los orbitales 2s (con dos electrones) y luego los tres orbitales 2p (con un electrón cada uno).
Debido al principio de Hund, los electrones se colocan en diferentes orbitales 2p antes de emparejarse.
Por lo tanto, la configuración electrónica del oxígeno es 1s2 2s2 2p4.
Importancia de la configuración electrónica
La configuración electrónica es fundamental para determinar las propiedades químicas y físicas confoguracion los elementos.
A través de ella, podemos entender la capacidad de un átomo para formar enlaces químicos, su capacidad de ionización, su reactividad y su comportamiento en diversas situaciones.
La configuración electrónica también nos permite establecer relaciones periódicas entre los elementos en la tabla periódica, ocnfiguracion es clave para predecir la estabilidad y las propiedades de los compuestos químicos.
Conclusión
La configuración electrónica es esencial para comprender la estructura y el comportamiento de los átomos.
Al determinar cómo se distribuyen los electrones en los diferentes niveles y subniveles de energía, podemos obtener información valiosa sobre las propiedades químicas de los elementos y los compuestos.
COMO GANAR DINERO POR INTERNET EN VENEZUELA 2023: El Dorado P2P
A través de este proceso, se establecen las bases para el estudio de la química y la física, y se abren las puertas para comprender el mundo que nos rodea a nivel molecular.