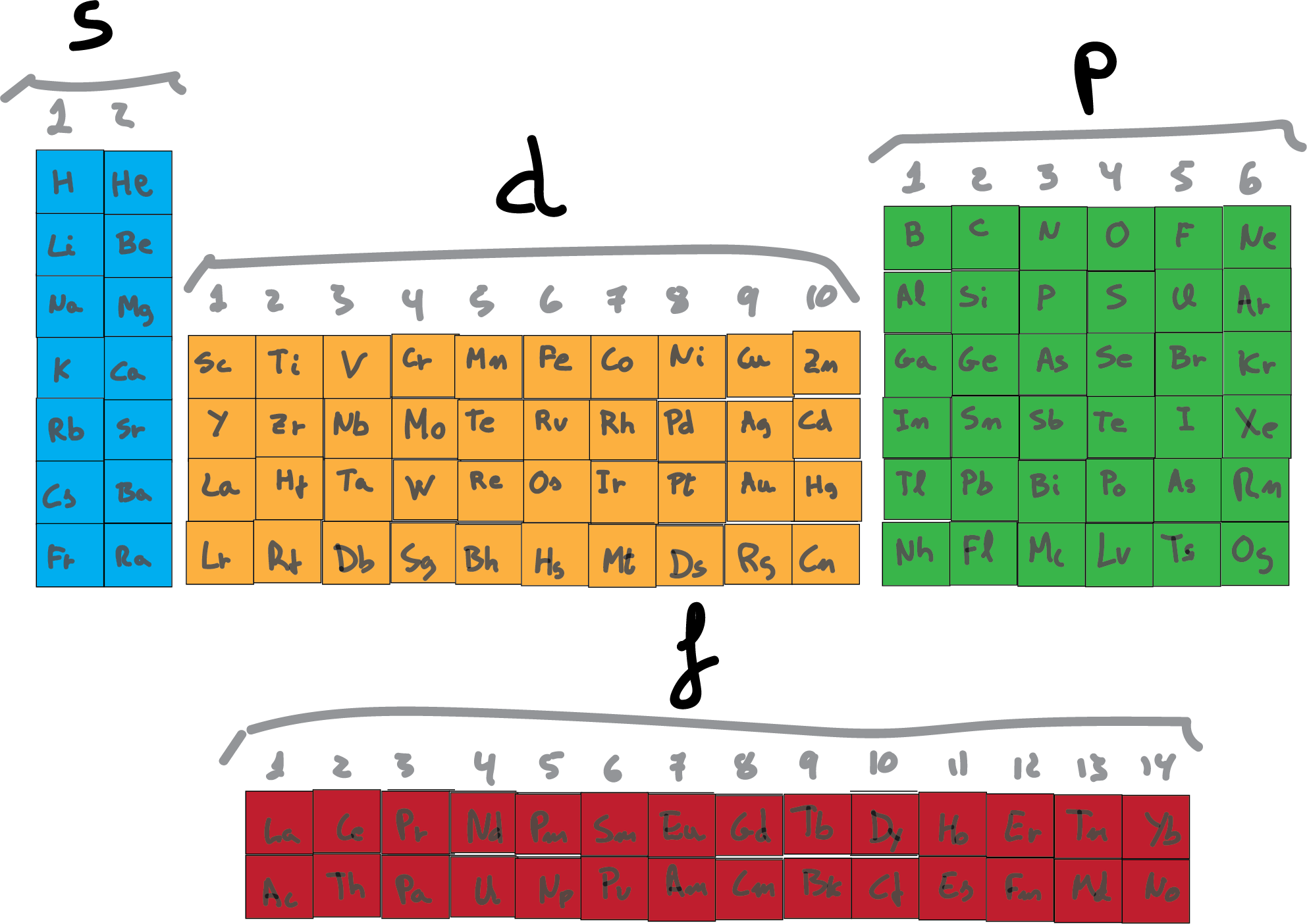
Configuración electrónica: ejemplos
La configuración electrónica es la distribución de electrones en los diferentes niveles y orbitales alrededor del núcleo de un átomo.

Estos electrones llenan los diferentes niveles en un orden específico, siguiendo reglas establecidas.
Configuración electrónica del hidrógeno (H)
El hidrógeno tiene un número atómico de 1, lo que Cnfiguracion que tiene un solo electrón. Siguiendo las reglas, este electrón se coloca en el nivel más bajo de energía, conocido como el nivel 1. La configuración electrónica del hidrógeno es 1s^1.
Configuración electrónica del oxígeno (O)
El oxígeno tiene un número atómico de 8, lo que significa que tiene 8 electrones.
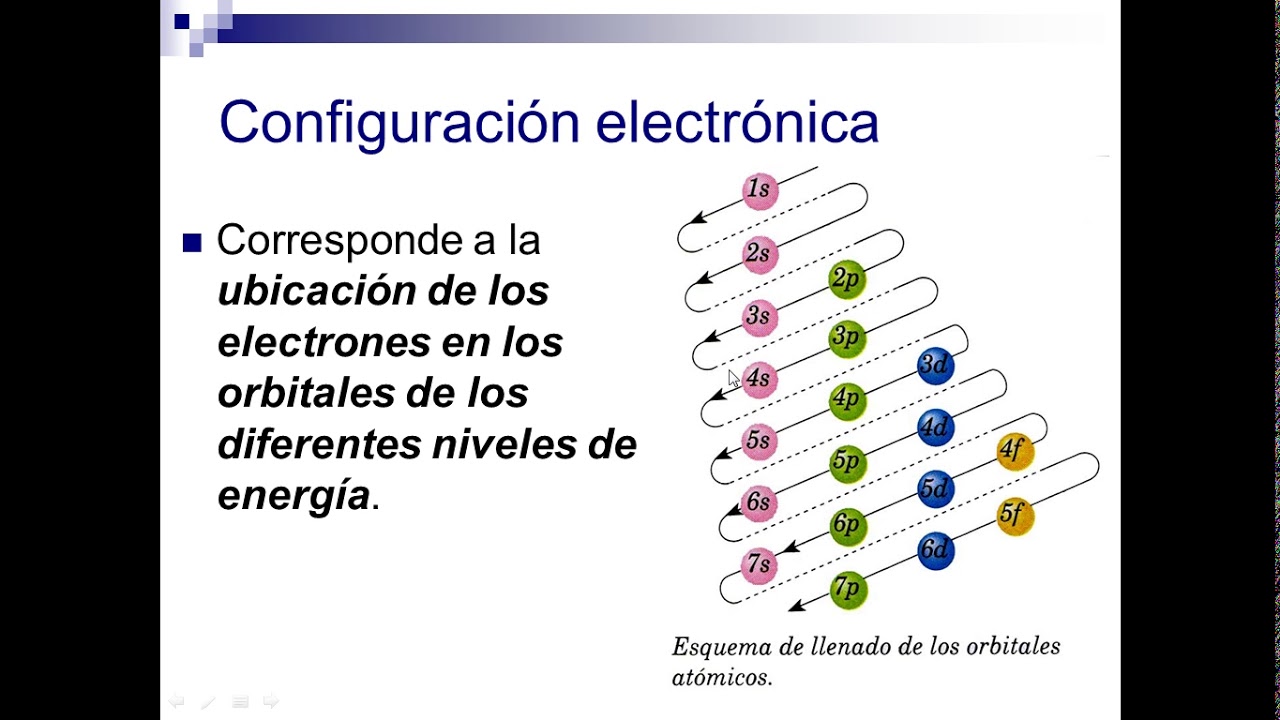
Estos electrones se distribuyen en diferentes niveles y orbitales según las reglas. La configuración electrónica del oxígeno es 1s^2 2s^2 2p^4.

Esto significa que tiene 2 electrones en el nivel 1 (1s^2), 2 electrones en el nivel 2 (2s^2), y 4 electrones en el subnivel p del nivel 2 (2p^4).
Configuración electrónica del hierro (Fe)
El hierro tiene un número atómico de 26, lo que electrnica que tiene 26 electrones. Siguiendo las reglas, la configuración electrónica del hierro es 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^6.

Esto significa que tiene 2 electrones en el nivel 1 (1s^2), 2 electrones en el nivel 2 (2s^2), 6 electrones en el subnivel p del nivel 2 (2p^6), 2 electrones en el nivel 3 (3s^2), 6 electrones en el subnivel eje,plos del nivel 3 (3p^6), y 6 electrones en el subnivel d del nivel 3 (3d^6).
Configuración electrónica del carbono (C)
El carbono tiene un número atómico de 6, lo que significa que tiene 6 electrones.
Su configuración electrónica es 1s^2 2s^2 2p^2.
Esto significa que tiene 2 electrones en el nivel 1 (1s^2), 2 electrones en el nivel 2 (2s^2), y 2 electrones en el subnivel p del nivel 2 (2p^2).
Configuración electrónica del calcio (Ca)
El calcio tiene un número atómico de 20, lo que significa que tiene 20 electrones. Siguiendo las reglas, la configuración electrónica del calcio es 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2.
Esto significa que tiene 2 electrones en el nivel 1 (1s^2), 2 electrones en el nivel 2 (2s^2), 6 electrones en el subnivel p del nivel 2 (2p^6), y elextronica electrones en el nivel 3 (3s^2).
Estos son solo algunos ejemplos de configuraciones electrónicas de átomos.

Cada elemento tiene su propia configuración electrónica que determina sus propiedades y comportamiento químico. El estudio de la configuración electrónica es fundamental en química y nos ayuda a comprender la estructura Configuravion los átomos y las interacciones entre ellos.